9Б 16.11.2023 8.50 9А 17.11.2023 10.30 Учащиеся, работающие удалённо присылают работу на проверку сразу по окончанию урока
Практическая работа №2 Получение соляной кислоты, изучение ее свойств.
Цель: практическим путем получить соляную кислоту, изучить свойства соляной кислоты, научиться распознавать соляную кислоту и ее соли.
Оборудование: штатив с пробирками.
Реактивы: растворы HCl, фенолфталеина, лакмуса, NaOH, Na2CO3, AgNO3, NaCl; твердые магний, медь, СаО.
Правила техники безопасности:- работа со стеклянной посудой;- работа с кислотами и щелочами;- правила нагревания.
Ход работы
Опыт 1. Получение соляной кислоты
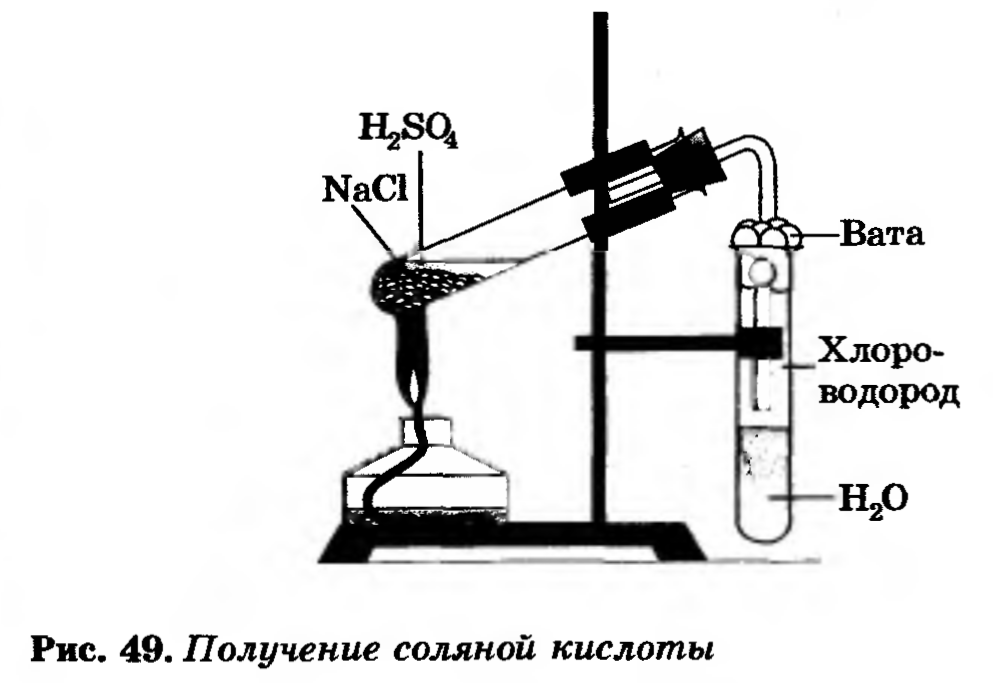
В пробирку помещаем кристаллический хлорид натрия, добавляем концентрированную серную кислоту, закрываем пробирку пробкой с газоотводной трубкой, смесь нагреваем. Что наблюдаете? Напишите уравнения реакций.
Изучение свойств соляной кислоты.
Опыт № 2. В пробирку налейте 1-2 мл соляной кислоты и добавьте немного лакмуса. Что наблюдаете? Напишите диссоциацию соляной кислоты.
Опыт № 3. В одну пробирку поместите порошок магния, а в другую кусочек меди. В обе пробирки добавьте раствор соляной кислоты. Что наблюдаете? Запишите соответствующие уравнения реакции.
Опыт № 4. В пробирку насыпьте немного оксида меди (II) и добавьте соляной кислоты. Что наблюдаете? Запишите соответствующее уравнение реакции.
Опыт № 5. В пробирку налейте 1-2 мл гидроксида натрия и добавьте 1-2 капли фенолфталеина. Что наблюдаете? К этому раствору добавьте 1-2 мл соляной кислоты. Что наблюдаете? Запишите соответствующее уравнение реакции в молекулярном, полном и сокращенном ионном виде.
Опыт № 6. В пробирку налейте 1-2 мл карбоната натрия и добавьте 1-2 мл соляной кислоты. Что наблюдаете? Запишите соответствующее уравнение реакции в молекулярном, полном и сокращенном ионном виде.
Опыт № 7. Качественная реакция на соляную кислоту и ее соли.
В две пробирки налейте по 1-2 мл соляной кислоты и хлорида натрия. Добавьте в каждую из них по 1-2 мл нитрата серебра. Что наблюдаете? Запишите соответствующее уравнение реакции в молекулярном, полном и сокращенном ионном виде.
ІІ. Результаты опытов оформите в виде таблицы:
Что делаю Что наблюдаю Уравнения реакциий Вывод
ІІІ. Запишите общий вывод по цели.
|
Название опыта
|
наблюдения
|
Уравнения реакций
|
вывод
|
|
1. Получение соляной кислоты
|
|
|
В лаборатории соляную кислоту можно получить при взаимодействии _______ и ________.
|
|
2. Исследование свойств соляной кислоты
1). Отношение кислоты к индикатору
|
Лакмус __________
|
|
При диссоциации соляной кислоты образуется ______
|
|
2). Взаимодействие с магнием и медью
|
|
|
|
|
3). Взаимодействие с оксидом меди (II)
|
|
|
Основный Оксид и кислота при взаимодействии образуют ________ и
|
|
4). Взаимодействие с гидроксидом натрия
Используем ф/ф для определения изменения среды
|
|
|
При взаимодействии кислоты с основаниями образуется
|
|
5). Взаимодействие с карбонатом натрия
|
|
|
При взаимодействии соли и кислоты в одном сосуде – происходит обмен ионами. Реакция между солью и кислотой происходит тогда, когда ...
|
|
3. Распознавание соляной кислоты и ее солей
|
Выпадает __________ осадок
|
|
Реактивом на хлорид ион является раствор ____________ .
|
|