Решение задач на вычисление массовой доли выхода продукта реакции
Повторить теоретический материал, решить предложенные для самостоятельной работы , задачи.
Расчетные задачи типа «Определение выхода продукта реакции в процентах от теоретического»
Признак В реальных химических реакциях масса продукта всегда оказывается меньше расчетной. Почему?
- Многие химические реакции обратимы и не доходят до конца.
- При взаимодействии органических веществ часто образуются побочные продукты.
- При гетерогенных реакциях вещества плохо перемешиваются, и часть веществ просто не вступает в реакции.
- Часть газообразных веществ может улетучиться.
- При получении осадков часть вещества может остаться в растворе.
Вывод:
- масса теоретическая всегда больше практической;
- объём теоретический всегда больше объёма практического.
Теоретический выход составляет 100%, практический выход всегда меньше 100%.
Количество продукта, рассчитанное по уравнению реакции, - теоретический выход, соответствует 100%.
В условии задачи встречается слово «выход». Теоретический выход продукта всегда выше практического.
Понятия «теоретическая масса или объём, практическая масса или объём» могут быть использованы только для веществ-продуктов.
Доля выхода продукта обозначается буквой
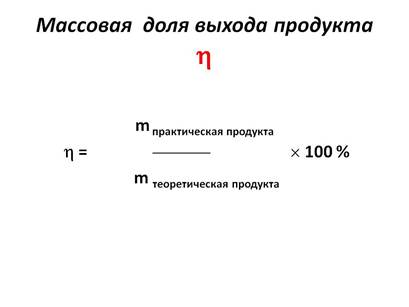 (эта), измеряется в процентах или долях. (эта), измеряется в процентах или долях.
Также для расчётов может использоваться количественный выход, исползуем отношение показателей количества вещества. В случае участия газов в реакции – отношение объёмов.
Задача 1. При взаимодействии магния массой 1,2 г с раствором серной кислоты получили соль массой 5, 5 г. Определите выход продукта реакции (%).
Второй тип задач
Известны масса (объём) исходного вещества (реагента) и выход (в %) продукта реакции. Необходимо найти практическую массу (объём) продукта реакции.
Задача 2. Вычислите массу карбида кальция, образовавшегося при действии угля на оксид кальция массой 16,8 г, если выход составляет 80%.
Третий тип задач
Известны масса (объём) практически полученного вещества и выход этого продукта реакции. Необходимо вычислить массу (объём) исходного вещества.
Задача 3. Карбонат натрия взаимодействует с соляной кислотой. Вычислите, какую массу карбоната натрия нужно взять для получения оксида углерода (IV) объёмом 28,56 л (н. у.). Практический выход продукта 85%.
|