Важнейшие соединения кальция (соли). Жёсткость воды и способы её устранения
Повторить п31 - общая характеристика металлов второй группы и их соединений.
Уч п32 составить конспект в тетради по вопросам:
- жёсткость воды
- особенности поведения катионов металлов первой и второй групп в растворах.
- записать в тетрадь все уравнения реакций с пояснениями.
- временная и постоянная жёсткость
- способы устранения . Почему жёсткость нужно устранять?
- что такое минеральная вода?
Природная вода, содержащая большое количество растворённых солей кальция и магния, называется жёсткой водой. Это названия возникло из-за того, что выстиранные в такой воде ткани становились грубыми из-за впитавшихся в них веществ.
Жёсткость воды и способы её устранения Растворимые соли кальция и магния присутствующие в природной воде обуславливают общую жёсткость воды. Если они присутствуют в воде в небольших количествах, то вода называется мягкой. При большом содержании этих солей (100 – 200 мг солей кальция – в 1 л в пересчёте на ионы) вода считается жёсткой. В такой воде мыло плохо пенится, так как соли кальция и магния образуют с ним нерастворимые соединения. В жёсткой воде плохо развариваются пищевые продукты, и при кипячении она даёт на стенках паровых котлов накипь. Накипь плохо проводит теплоту, вызывает увеличение расхода топлива и ускоряет изнашивание стенок котла. Жёсткость, вызванная присутствием в воде гидрокарбонатов кальция и магния, называется карбонатной или временной, так как она устраняется при кипячении. Помимо карбонатной жёсткости, различают ещё некарбонатную жёсткость, которая зависит от содержания в воде сульфатов и хлоридов кальция и магния. Эти соли не удаляются при кипячении, и поэтому некарбонатную жёсткость называют также постоянной жёсткостью. Карбонатная и некарбонатная жёсткость в сумме даёт общую жёсткость. Для устранения карбонатной жёсткости воду кипятят. Общую жёсткость устраняют или добавлением химических веществ, или при помощи так называемых катионитов. При использовании химического метода растворимые соли кальция и магния переводят в нерастворимые карбонаты, например, добавляют известковое молоко и соду.
|
Жесткость воды и способы ее устранения
|
|
Состав жесткой воды
|
Вид жесткости
|
Способы устранения
|
|
катионы
|
анионы
|
по составу
|
по способу её устранения
|
|
Са 2 +
Mg 2+
|
НСО-3
|
карбонатная
|
временная
|
1) нагревание
2) добавление известкового молока или соды.
|
|
Сl -
SO42-
|
некарбонатная
|
постоянная
|
1) добавление соды
|
|
НСО-3
Сl -
SO42-
|
общая
|
1) добавление соды
2) добавление извести
|
Временную (карбонатную) жёсткость устраняют:
1. Кипячением Са(НСО3)2 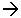 СаСО3 + Н2О + СО2 СаСО3 + Н2О + СО2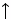
Mg(НСО3)2 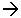 Mg(OH)2 + 2СО2 Mg(OH)2 + 2СО2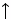
При длительном кипячении растворимые Са(НСО3)2 и Mg(НСО3)2 переходят в нерастворимые соединения и выпадают в осадок. Поэтому карбонатную жёсткость называют также временной жёсткостью. Количественно временную жёсткость характеризуют содержанием гидрокарбонатов, удаляющихся из воды при её кипячении в течение часа. Жёсткость, остающаяся после такого кипячения, называется постоянной.
2. Добавлением гашёной извести.
Са(НСО3)2 + Са(ОН)2 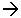 2CaCO3 2CaCO3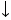 + 2H2O + 2H2O
Mg(НСО3)2 + 2Са(ОН)2 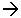 Mg(OH)2 Mg(OH)2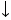 + 2CaCO3 + 2CaCO3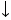 + 2H2O + 2H2O
Постоянную (некарбонатную) жёсткость устраняют добавлением соды Na2CO3.
CaCl2 + Na2CO3 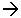 CaCO3 CaCO3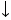 + 2NaCl + 2NaCl
MgSO4 + Na2CO3 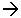 MgCO3 MgCO3 + Na2SO4 + Na2SO4
В целях одновременного устранения обоих видов жёсткости применяют смесь гашёной извести и соды – содово-известковый метод.
|