Применение кислорода. Способы получения кислорода в промышленности и лаборатории. Круговорот кислорода в природе.
Учить §13 стр 63 и 65. Подготовить практическую работу стр 68 часть 1 ( изучить, разобрать какие процессы проходят, найти видео, посмотреть, выучить теоретический материал)
Кислород – это сознание человека. Он особенно необходим мозгу. Клетки мозга разлагаются и умирают без кислорода гораздо быстрее других клеток организма.
62% массы человека – это масса всех атомов кислорода, входящих в состав тела.
Кислород входит в состав органических соединений: белков, жиров, углеводов, витаминов, ферментов, гормонов.
Высокая окислительная способность кислорода лежит в основе горения всех видов топлива.
Электрические и тепловые станции, работающие на угле, нефти или природном газе используют атмосферный кислород для сжигания топлива.
В медицине кислород используют для поддержания жизни больных с затрудненным дыханием и для лечения некоторых заболеваний. Однако чистым кислородом при нормальном давлении долго дышать нельзя – это опасно для здоровья.
Вне земной атмосферы человек вынужден брать с собой запас кислорода. Мы уже говорили о его применении на подводных лодках.
В лаборатории кислород получают разложением некоторых кислородсодержащих веществ. Собирают его вытеснением воды или воздуха.
Разложение марганцовки (перманганата калия) при нагревании:
2KMnO4=tK2MnO4+MnO2+O2.
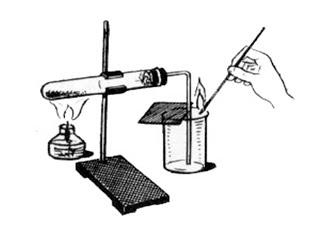
Способ Разложение перманганата калия будет использован на следующем уроке во время практической работы. Этот рисунок вы должны будете выполнить в тетради для практических работ. Изучите его. Какой метод сбора кислорода был использован?
2H2O2=2H2O+O2.
Электролиз воды: 2H2O=эл. ток2H2+O2.
Можно получить кислород и при разложении некоторых других веществ: бертолетовой соли KClO3, нитратов NaNO3, KNO3 и т. д.
- В промышленных масштабах кислород получают из воздуха. Для этого воздух при повышенном давлении охлаждают и превращают в жидкость. Затем жидкий воздух нагревают. Сначала выделяется азот (температура кипения –196 °С). Жидкий
- кислород остаётся, так как его температура
- кипения выше (–183 °С). Хранят жидкий кислород в стальных баллонах голубого цвета.
Применение кислорода
- Все области применения кислорода основаны в основном на физических свойствах кислорода . Главными потребителями кислорода, конечно, являются энергетика, металлургия и химическая промышленность.
- В металлургической промышленности кислород используется при выплавке чугуна и стали.
- В смеси с водородом или ацетиленом кислород применяется для резки и сварки металлов. Горючий газ ацетилен, сгорая в токе кислорода, позволяет получить температуру выше 3000°С
- Находит применение кислород в качестве окислителя ракетного топлива.
- Используется он для обеспечения жизнедеятельности на подводных лодках и космических кораблях, при работе водолазов.
- Находит применение в медицине в лечебных целях. В медицине кислород тоже нашел свое применение. Кислород используется для обогащения дыхательных газовых смесей при нарушении дыхания, для лечения астмы, профилактики гипоксии в виде кислородных коктейлей, кислородных подушек. Однако чистым кислородом при нормальном давлении долго дышать нельзя – это опасно для здоровья.
Кислород выполняет бесценную биологическую роль.Кислород необходим практически всем живым существам для дыхания. Дыхание – это окислительно-восстановительный процесс, где кислород является окислителем. С помощью дыхания живые существа вырабатывают энергию, необходимую для поддержания жизни.
https://www.youtube.com/watch?v=iSpi9Zs-xMA Круговорот кислорода в природе
Посмотреть сюжет, а также внимательно изучить рис 47 стр 65
|