Аминокислоты и белки. Состав и номенклатура. Аминокислоты как амфотерные органические соединения. Пептидная связь. Биологическое значение альфа- аминокислот. Области применения.
Учить п19, аминокислоты. Состав, строение , структура, свойства .
В 1820 г. французский химик Анри Браконно проводил опыты с веществами животного происхождения. В результате длительного нагревания кожи, хрящей и сухожилий с раствором серной кислоты он получил некоторое количество белых кристаллов сладкого вкуса. Какой тип реакций протекал при этом?
Ученик: Очевидно, реакции гидролиза, катализируемые сильной кислотой.
Учитель: Это вещество получило название гликокол, оно долгое время считалось «родственником» углеводов, пока в 1838г. голландский химик Г.Мульдер не обнаружил в его составе азот. Спустя ещё 6 лет Э.Хорсфорд установил формулу вещества – C2H5O2N. Это глицин.
Аминокислоты – производные карбоновых кислот , у которых один или несколько атомов водорода замещены на аминогруппы.
Простейший представитель Аминоуксусная кислота (аминоэтановая кислота или глицин). NH2 – CH2 – COOH
https://yandex.fr/video/preview/17717178722868449429 аминокислоты и белки
https://yandex.fr/video/preview/10179881542517006296 аминокислоты + номенклатура и изомерия
Содержат в составе 2 функциональные группы - NH2 – амино, - COOH – карбоксильная
Аминокислоты классифицируют по происхождению, в связи с чем их делят на: природные и синтетические.
Природные
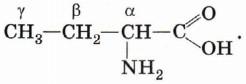
Их около 150, они были обнаружены в живых организмах, около 20 из них входят в состав белков. Половина этих аминокислот – незаменимые (не синтезируются в организме человека), поступают с пищей. Это Альфа- аминокислоты, хотя работа нервной системы связана с участием ℽ-аминомасляной кислоты.
Синтетические
Получают кислотным гидролизом белков, либо из карбоновых кислот, воздействуя на них галогеном, а затем аммиаком.
Природные аминокислоты можно разделить на следующие основные группы:
- Алифатические предельные - глицин, аланин
- серосодержащие - цистеин
-содержащие гидроксильную группу – серин, фенилаланин
- ароматические – фенилаланин, тирозин
- с двумя карбоксильными группами – глутаминовая кислота
- с двумя аминогруппами – лизин
Физические свойства: бесцветные кристаллические вещества с температурами плавления 150 - 250oС, хорошо растворимы в воде (лучше, чем в органических растворителях), многие - сладкие.
Как называются вещества, которые взаимодействуют и с кислотами и со щелочами?
Общая формула молекул аминокислот - NH2—R—COOH, где R - двухвалентный радикал. В твердом состоянии и частично в растворах аминокислоты представляют собой "внутренние соли", то есть состоят из биполярных ионов +NH3—R—COO-, образующихся при обратимом переносе протона (H+) от карбоксильной группы к аминогруппе, например:
Аминокислоты – твердые кристаллические вещества с высокой температурой плавления. Хорошо растворимы в воде, водные растворы хорошо проводят электрический ток.
1) Реакции с растворами кислот:
NH2CH2COOH + HCl →(NH3CH2COOH)Cl
2) Реакции с растворами щелочей или металлами:
NH2CH2COOH + NaOH → NH2CH2COONa + H2O (аминоацетат натрия)
Аминокислоты - амфотерные органические вещества. В водных растворах большинства аминокислот среда слабокислотная, у лизина - слабощелочная.
Так как аминокислоты в водных растворах ведут себя как типичные амфотерные соединения, то в живых организмах они играют роль буферных веществ, поддерживающих определённую концентрацию ионов водорода.
3) Реакция горения 4NH2CH2COOH + 13O2 → 8CO2 + 10H2O + 2N2
4) Реакцию поликонденсации аминокислот или межмолекулярного взаимодействия.
Группа —CO—NH— называется амидной группой, а образующиеся полимеры - полиамидами. Полиамиды -аминокислот называются пептидами. В зависимости от числа остатков аминокислот различают дипептиды, трипептиды, полипептиды. В таких соединениях группы —CO—NH— называют пептидными группами, а связь C—N - пептидной связью. Полипептиды называют также белками или протеинами.
5) Общая формула молекул аминокислот - NH2—R—COOH, где R - двухвалентный радикал. В растворах аминокислоты представляют собой "внутренние соли", то есть состоят из биполярных ионов +NH3—R—COO-, образующихся при обратимом переносе протона (H+) от карбоксильной группы к аминогруппе.
6) Взаимодействие с аминами с образованием солей или амидов.
7) Реакция эстерификации со спиртами
В 1806 г. французские химики Луи Никола Воклен и Пьер Жан Робике исследовали состав сока некоторых растений. Из сока спаржи им удалось выделить белое кристаллическое вещество, названное ими аспарагином (от греческого названия спаржи — asparagus). Это была первая аминокислота, выделенная химиками из природных объектов. В 1848 г. итальянец Рафаэль Пириа обнаружил, что гидролизом аспарагина можно получить аспарагиновую кислоту
В живых организмах аспарагиновая кислота, напротив, связывает токсичный аммиак, превращаясь в аспарагин.
Из белка, содержащегося в зернах пшеницы, была выделена очень похожая по строению на аспарагиновую кислота, названная глутаминовой (от лат, gluten — клейковина). В значительных количествах она содержится в мозге, сердечной мышце и плазме крови. Она также способна взаимодействовать с аммиаком, превращаясь в амид — глутамин
Это свойство глутаминовой кислоты используют при лечении некоторых заболеваний (шизофрении, эпилепсии).
Еще одно неожиданное свойство аминокислот. Предприимчивые японцы давно заметили, что добавление в пищу приправы из сушеных водорослей усиливает ее вкус и аромат. В 1909 г. японский ученый К. Икеда выяснил, что причина такого действия приправы кроется в содержащихся в водорослях глутаминовой кислоте и ее солях. К. Икеда запатентовал свое открытие, и теперь во всем мире в качестве пищевых добавок, усиливающих вкус и аромат продукта, используют глутаминовую кислоту (Е620), глутаминат натрия (Е621, часто называют глютамат натрия) и глутаминаты других металлов (Е622—Е625). Ссылки на эти вещества легко найти, например, на баночке мясного паштета. Для тех же целей применяют глицин (Е640) и лейцин (Е641)
|