Амины. Строение молекул аминов. Номенклатура. Физические свойства. Химические свойства алифатических аминов на примере метиламина.
Уч п18
Серотонин улучшает аппетит, повышает настроение и контролирует эмоции человека. Адреналин стимулирует центральную нервную систему. Все эти соединения – амины. Без них невозможно представить жизнь человека. Амины – углеводородные производные аммиака, в которых вместо водородных атомов располагаются радикалы. Функциональная группа аминов: аминогруппа (-NH2).
французский ученый Ш.Вюрц в 1849 году в продуктах гидролиза азотсодержащих природных веществ обнаружил «летучие органические основания» - амины.
Русский ученый Ю.Ф. Фрицше в 1840 году получил анилин при нагревании природного красителя синего цвета индиго. Он же обнаружил, что при окислении анилина образуются интенсивно окрашенные вещества, поэтому анилин применяют для окраски ткани.
Русский ученый Николай Николаевич Зинин в 1842 году в одной из научных статей сообщил, что при небольшом нагревании нитробензола с сероводородной кислотой или сульфидом аммония образуется «восстановительный нитробензол» – анилин. Это открытие явилось мощным фактором развития химической промышленности.
Амины – производные углеводородов, в которых атом водорода замещен на аминогруппу –NH2.
С другой стороны, их можно представить как продукты замещения атомов водорода в молекуле аммиака на органические радикалы.
СnH2n+3N
В зависимости от числа замещенных атомов различают первичные, например метиламин CH3NH2, вторичные, такие, как диэтиламин(C2H5)2NH, и третичные амины, примером которых может быть диметилэтиламин(CH3)2(C2H5)N. Из последнего примера видно, что присоединенные к атому азота группы могут быть неодинаковыми.
Сходство аминов с аммиаком не формальное. Эти вещества имеют схожие свойства, в частности и аммиак, и амины проявляют основные свойства (слабые основания).
Названия аминов производят от названия радикалов, входящих в молекулу, с добавлением окончания -амин:
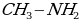 метиламин, метиламин,
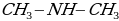 диметиламин, диметиламин,
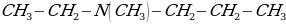 метилэтилпропиламин метилэтилпропиламин
Алифатические - метиламин, диметиламин…
Ароматические - фениламин
Смешанные - метилфениламин
Для аминов можно выделить 3 типа изомерии:
1.Изомерия углеродного скелета:
CH3-CH(CH3)- CH2-NH2 изобутиламин
2.Изомерия положения функциональной группы:
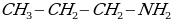 пропиламин-1 пропиламин-1
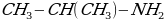 пропиламин-2 пропиламин-2
3.Изомерия между типами аминов:
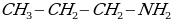 первичный амин первичный амин
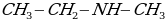 вторичный амин вторичный амин
По физическим свойствам:
- Низшие амины при нормальных условиях – газы, имеющие запах аммиака
- Средние – жидкости со слабым запахом аммиака
- Высшие – твердые вещества без запаха
Метиламин, диметиламин и триметиламин — газообразные вещества, с запахом аммиака, хорошо растворяются в воде, так как их молекулы образуют водородные связи с молекулами воды.
Средние члены алифатического ряда – жидкости со слабым запахом тухлой рыбы, с постепенно повышающейся температурой кипения.
Высшие амины (начиная с С16Н35N — твердые нерастворимые вещества, не имеющие запаха.
Ароматические амины – бесцветные высококипящие жидкости или твердые вещества, практически нерастворимые в воде.
Связь N–H является полярной, поэтому первичные и вторичные амины образуют межмолекулярные водородные связи (несколько более слабые, чем Н-связи с участием группы О–Н).Это объясняет относительно высокую температуру кипения аминов по сравнению с неполярными соединениями со сходной молекулярной массой.
Анилин (фениламин) С6H5NH2 – важнейший из ароматических аминов:
Анилин представляет собой бесцветную маслянистую жидкость с характерным запахом (т. кип. 184 °С, т. пл. – 6 °С). На воздухе быстро окисляется и приобретает красно-бурую окраску. Ядовит.

Атом азота находится в состоянии sp3-гибридизации, поэтому молекула имеет форму тетраэдра.
Также атом азота в аминах имеет неподелённую электронную пару, поэтому амины проявляют свойства органических оснований. Донорно- акцепторная связь
Химические свойства
1.взаимодействие с кислотами:
Так как амины основания, то они, как и аммиак, вступают в реакцию с кислотами. При этом образуются соли.
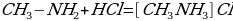 хлорид метиламмония хлорид метиламмония
2. взаимодействие с водой:
При взаимодействии с водой амины, как и аммиак, присоединяют протон (ион водорода Н+) по месту свободной неподеленной пары атома азота, что ведет к накоплению гидроксид-ионов в растворе. Поэтому растворы аминов проявляют щелочную реакцию. Индикаторы изменяют свою окраску в растворах аминов следующим образом: лакмус – синий, метилоранж – желтый, фенолфталеин – малиновый.
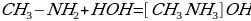 гидроксид метиаммония гидроксид метиаммония
3.Амины горят на воздухе с образованием углекислого газа и, воды и азота:
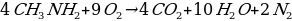
4.Реакция галогенирования:
Амины, как и алканы, вступают в реакции замещения с галогенами
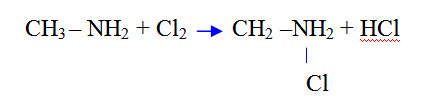
Основные свойства в ряду метиламин →аммиак→анилин ослабевают.
Получение :
Гидрирование водородом нитросоединений R-NO2 + 3H2 = R-NH2 + 2H2O
Анилин ядовит! Действуя на центральную нервную систему, он вызывает в крови образование метгемоглобина и дегенеративные изменения эритроцитов, гемолиз, следствием чего является кислородное голодание организма.
Анилин проникает в организм через органы дыхания в виде паров, а также при всасывании через кожу и слизистые оболочки, которое особенно усиливается при повышении температуры воздуха и приёме алкоголя. Возможны острые и хронические (анилизм) отравления анилином. При лёгком отравлении анилином наблюдаются слабость, головокружение, головная боль, синюшность губ, ушных раковин, ногтей. При отравлениях средней тяжести присоединяется тошнота, иногда рвота, появляется шатающаяся походка, учащённый пульс. При хронических отравлениях возможен токсический гепатит, нервно-психические нарушения, расстройство сна, снижение памяти и т. д.
|